A autorização de medicamentos experimentais no exterior é um tema cada vez mais relevante para pacientes, médicos e famílias que buscam alternativas terapêuticas quando os tratamentos convencionais não apresentam resultados satisfatórios.
Entender como funciona esse processo é fundamental para evitar atrasos, riscos regulatórios e frustrações ao longo do caminho.
Neste artigo, você vai entender como funciona a autorização de medicamentos experimentais, quais são os órgãos envolvidos, os principais modelos regulatórios internacionais, os documentos exigidos e os desafios mais comuns.
O que são medicamentos experimentais
Medicamentos experimentais são aqueles que ainda não possuem registro comercial definitivo em determinado país. Em geral, eles estão em uma das seguintes situações:
- Em fase de pesquisa clínica
- Aprovados para uso restrito em estudos
- Autorizados apenas para uso compassivo
- Disponíveis apenas em mercados específicos
Mesmo sem registro definitivo, esses medicamentos podem ser utilizados legalmente em situações específicas, desde que exista uma autorização de medicamentos experimentais concedida pelas autoridades competentes.
Quando a autorização de medicamentos experimentais é necessária
A autorização medicamentos experimentais é exigida sempre que:
- O medicamento não possui registro no país de destino
- O uso será feito fora de um estudo clínico formal
- O tratamento é destinado a um paciente específico
- Não há alternativa terapêutica equivalente disponível
Esse tipo de autorização costuma ser solicitado em casos de doenças raras, câncer, condições neurológicas, genéticas ou enfermidades em estágio avançado.
Quem regula a autorização de medicamentos experimentais no exterior
Cada país possui sua própria agência reguladora responsável por avaliar pedidos de autorização de medicamentos experimentais. As mais conhecidas incluem:
- Food and Drug Administration (Estados Unidos)
- European Medicines Agency (União Europeia)
- Agência Nacional de Vigilância Sanitária (Brasil)
Apesar das diferenças entre os sistemas, o objetivo é o mesmo: garantir segurança, rastreabilidade e justificativa médica para o uso do medicamento.
Principais modelos de autorização de medicamentos experimentais
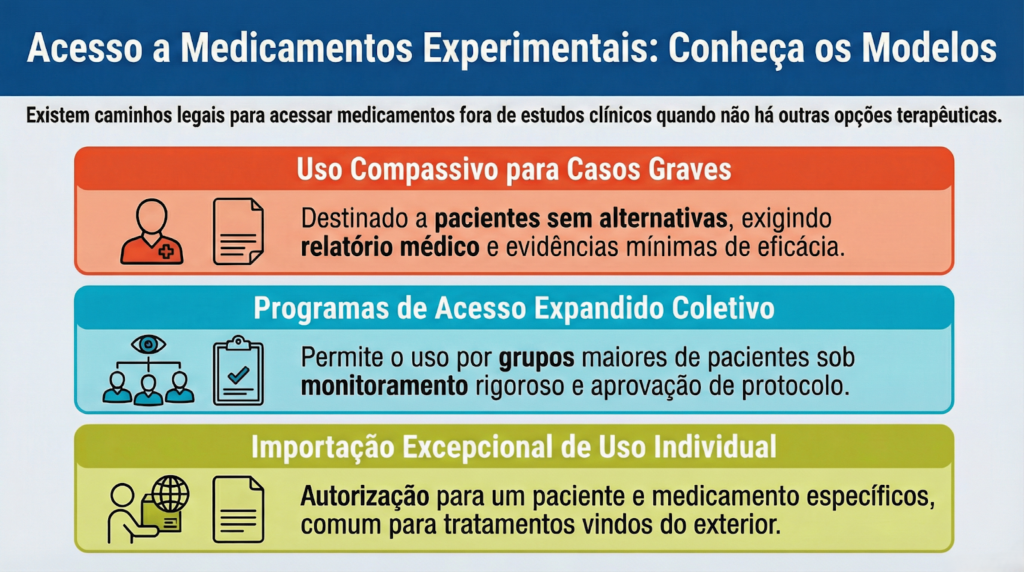
Uso compassivo
O uso compassivo permite que um paciente tenha acesso a um medicamento experimental fora de um estudo clínico, geralmente em situações graves ou sem opções terapêuticas.
Para obter a autorização de medicamentos experimentais nesse modelo, normalmente é necessário:
- Relatório médico detalhado
- Justificativa clínica
- Evidências científicas mínimas de eficácia
- Consentimento informado do paciente
Programas de acesso expandido
Alguns países adotam programas de acesso expandido, que permitem o uso de medicamentos ainda em pesquisa por grupos maiores de pacientes.
Nesse caso, a autorização de medicamentos experimentais envolve:
- Aprovação prévia do protocolo
- Controle rigoroso de uso
- Monitoramento de efeitos adversos
Importação excepcional para uso individual
Esse é um dos modelos mais comuns para pacientes que buscam tratamento no exterior. A autorização de medicamentos experimentais é concedida para:
- Um paciente específico
- Um medicamento específico
- Um período determinado de tratamento
Esse modelo costuma exigir menos etapas do que estudos clínicos formais, mas ainda demanda documentação completa.
Documentos exigidos no processo de autorização
Embora os requisitos variem de país para país, a autorização de medicamentos experimentais geralmente exige:
- Prescrição médica detalhada
- Relatório clínico justificando o uso
- Dados do medicamento (fabricante, composição, fase de estudo)
- Termo de responsabilidade
- Documentação do paciente
A ausência ou inconsistência em qualquer um desses documentos pode atrasar ou inviabilizar a autorização.
Etapas do processo de autorização de medicamentos experimentais
A seguir, um panorama geral do fluxo de autorização medicamentos experimentais no exterior:
| Etapa | Descrição |
| Avaliação médica | Análise da necessidade clínica do medicamento |
| Reunião de documentos | Prescrição, laudos e justificativas |
| Submissão regulatória | Envio do pedido à autoridade competente |
| Análise técnica | Avaliação de segurança e viabilidade |
| Decisão | Aprovação, solicitação de ajustes ou negativa |
| Liberação logística | Autorização para envio e uso do medicamento |
Esse processo pode levar de dias a algumas semanas, dependendo do país, da urgência clínica e da qualidade da documentação apresentada.
Diferença entre autorização no país de origem e no país de destino
Um ponto importante é entender que a autorização de medicamentos experimentais não é automática entre países. Um medicamento autorizado nos Estados Unidos, por exemplo, não está automaticamente liberado para uso em outro país.
Cada autoridade reguladora avalia:
- Riscos ao paciente
- Evidências científicas disponíveis
- Contexto clínico individual
Por isso, o processo deve ser conduzido de forma estratégica e alinhada às exigências locais.
Riscos de tentar importar medicamentos experimentais sem autorização
Ignorar a autorização de medicamentos experimentais pode gerar consequências sérias, como:
- Retenção do medicamento na alfândega
- Multas e sanções administrativas
- Perda do medicamento
- Atrasos críticos no tratamento
Além disso, o uso sem autorização pode colocar o paciente em situação de vulnerabilidade jurídica e sanitária.
A importância de suporte especializado no processo
A autorização de medicamentos experimentais envolve aspectos médicos, regulatórios e logísticos. Por isso, contar com suporte especializado reduz riscos e aumenta significativamente as chances de sucesso.
Um acompanhamento adequado ajuda a:
- Definir o melhor modelo de autorização
- Evitar retrabalho documental
- Reduzir prazos
- Garantir conformidade regulatória
Esse tipo de suporte é especialmente importante em tratamentos de alto custo ou com caráter de urgência.
Tendências atuais na autorização de medicamentos experimentais
Nos últimos anos, as autoridades regulatórias têm buscado:
- Processos mais digitais
- Análises mais rápidas para casos graves
- Maior integração entre dados clínicos e regulatórios
Mesmo assim, a autorização de medicamentos experimentais continua sendo um processo técnico, que exige planejamento e precisão.
Como a Flymed pode ajudar nesse processo
A Flymed atua no suporte completo para pacientes e famílias que precisam entender e viabilizar a autorização de medicamentos experimentais no exterior, cuidando desde a análise documental até a logística internacional.
Se você ou alguém próximo enfrenta a necessidade de acesso a um medicamento experimental, conheça as soluções da Flymed e entenda como transformar um processo complexo em um caminho mais seguro, organizado e transparente.
👉 Acesse agora: https://flymed.com.br/
